
Зустрічаються наївні люди, які стверджують, що за мільярди років еволюції природа так і не винайшла колесо. Якби вони зменшилися до нанорівня та здійснили подорож всередину живої клітини, то побачили б не тільки колесо, а й електродвигуни, конвеєри, складальні лінії та навіть крокуючих роботів, передають Патріоти України з посиланням на Нескучные новости.
За підрахунками біологів, у живій клітині функціонує близько сорока відомих науці молекулярних машин. Вони возять вантажі по молекулярним «рейкам», виступають у якості «вмикачів» та «вимикачів» хімічних процесів. Машини з молекул виробляють енергію для підтримки життя, скорочують наші м'язи та будують інші молекулярні машини. А ще вони надихають учених на будівництво рукотворних нанороботів, які у майбутньому зможуть жити та працювати у внутрішньоклітинному світі. Далі мовою першоджерела.
Известный российский биохимик, академик РАН Владимир Скулачёв назвал движение бактерий одним из самых поразительных явлений природы: «Его исследование нанесло сокрушительный удар по нашему высокомерному снобизму вроде того, что биологическая эволюция, имея в своем распоряжении миллиарды лет, так и не смогла изобрести колесо».
Для передвижения в жидкой среде некоторые бактерии используют вращающийся жгутик, который приводится микроскопическим электродвигателем, собранным из нескольких белковых молекул. Раскручиваясь до 1000 об/мин, жгутик может толкать бактерию вперед с необыкновенно большой скоростью — 100−150 мкм/с. За секунду одноклеточное перемещается на расстояние, превосходящее его длину более чем в 50 раз. Если это перевести на привычные нам величины, то спортсмен-пловец ростом в 180 см должен был бы переплывать 50-метровый бассейн за полсекунды!
Метаболизм бактерии устроен таким образом, что положительные ионы водорода (протоны) накапливаются между внутренней и внешней мембранами ее клетки. Создается электрохимический потенциал, увлекающий протоны из межмембранного пространства в клетку. Этот поток протонов проходит через «двигатель», приводя его в движение.
Белковую структуру «мотора» называют комплексом Mot, который, в свою очередь, состоит из белков Mot A (статора) и Mot B (ротора). Ионные каналы в них расположены таким образом, что движение протонов заставляет ротор вращаться подобно турбине. Манипулируя структурой белка, некоторые бактерии умеют изменять направление и скорость движения, а иногда даже включать «задний ход».
Наличие вращающихся частей у живого организма поначалу казалось столь невероятным, что потребовало серьезных экспериментальных подтверждений. Таких подтверждений было получено несколько. Так, в лаборатории академика Скулачёва бактерию характерной формы (в виде полумесяца, где передняя часть бактерии была вогнутой, задняя — выпуклой) прикрепляли жгутиком к стеклу и наблюдали за ней в микроскоп. Было хорошо видно, как бактерия вращается, постоянно показывая наблюдателю лишь переднюю часть, свою «впалую грудь», и никогда не поворачиваясь «спиной».
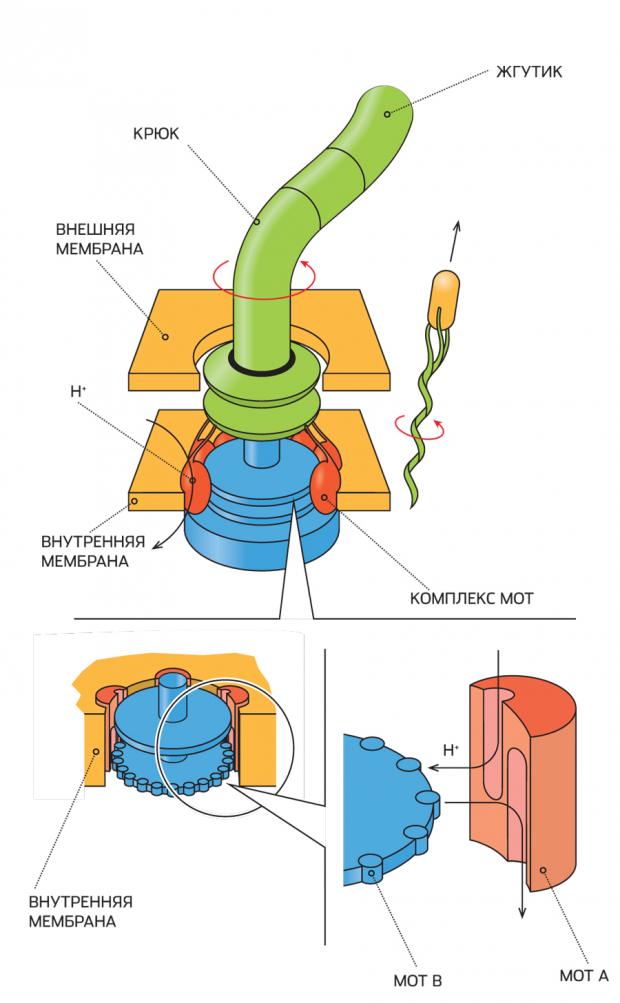
Схема «электродвигателя» бактерии гораздо больше напоминает инженерный чертеж, чем изображение живого организма. Главная деталь «мотора» — белок Mot A с ионными каналами, благодаря которым поток протонов заставляет ротор вращаться, как турбина.
Протонная АТФ-синтаза — самый маленький в живой природе биологический мотор шириной всего в 10 нм. С его помощью живые организмы вырабатывают аденозинтрифосфат (АТФ) — вещество, которое служит основным источником энергии в клетке.
АТФ состоит из аденозина (соединение хорошо знакомого нам по ДНК азотистого основания аденина и сахара рибозы и трех последовательно подсоединенных к нему фосфатных групп. Химические связи между фосфатными группами очень сильные и содержат много энергии. Эта консервированная энергия может пригодиться для питания самых разнообразных биохимических реакций. Однако сперва необходимо определенным образом приложить энергию, чтобы упаковать аденозин и фосфатные группы в молекулу АТФ. Этим и занимается АТФ-синтаза.
Поступающие в организм жирные кислоты и глюкоза проходят многочисленные циклы, в процессе которых специальные ферменты дыхательной цепи откачивают положительные ионы водорода (протоны) в межмембранное пространство. Там протоны накапливаются, как войско перед битвой. Создается потенциал: электрический (положительные заряды снаружи митохондриальной мембраны, отрицательные внутри органеллы) и химический (возникает разница концентраций ионов водорода: внутри митохондрии их меньше, снаружи больше).
Известно, что электрический потенциал на мембране митохондрий, которая служит хорошим диэлектриком, достигает 200 мВ при толщине мембраны всего 10 нм.
Накопившись в межмембранном пространстве, протоны, подобно электрическому току, устремляются назад, в митохондрию. Они проходят по специальным каналам в АТФ-синтазе, которая встроена во внутреннюю сторону мембраны. Поток протонов раскручивает ротор, будто река водяную мельницу. Ротор вращается со скоростью 300 оборотов в секунду, что сопоставимо с максимальными оборотами двигателя болида «Формулы-1». АТФ-синтазу по форме можно сравнить с грибом, «растущим» на внутренней стороне мембраны митохондрии, при этом описанный выше ротор прячется в «грибнице». «Ножка гриба» вращается вместе с ротором, и на ее конце (внутри «шляпки») закреплено некое подобие эксцентрика. Неподвижная «шляпка» условно делится на три дольки, каждая из которых деформируется, сжимается при прохождении эксцентрика. К «долькам» прикрепляются молекулы аденозиндифосфата (АДФ, с двумя фосфатными группами) и остатки фосфорной кислоты. В момент сжатия АДФ и фосфат прижимаются друг к другу достаточно сильно, чтобы образовать химическую связь. За один оборот «эксцентрик» деформирует три «дольки», и образуется три молекулы АТФ. Помножив это на количество секунд в сутках и примерное количество АТФ-синтаз в организме, мы получим удивительную цифру: ежедневно в человеческом теле вырабатывается примерно 50 кг АТФ.
Все тонкости этого процесса необычайно сложны и многообразны. За их расшифровку, которая потребовала почти ста лет, были вручены две Нобелевские премии — в 1978 году Питеру Митчеллу и в 1997 году Джону Уокеру и Полю Бойеру.
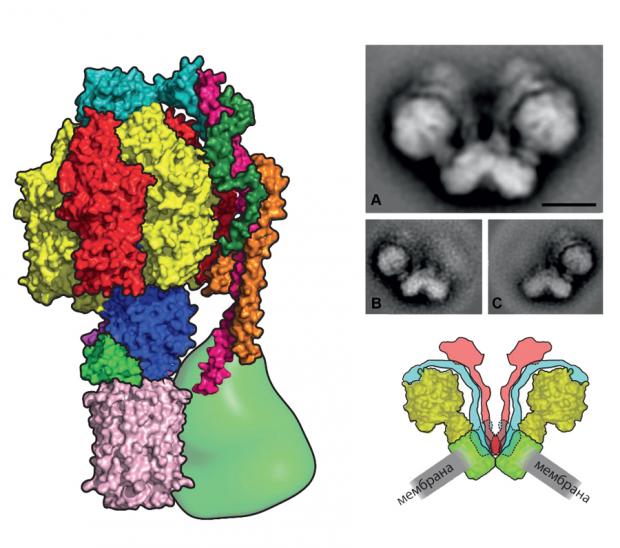
Как и в случае со жгутиками бактерий, движение ротора АТФ-синтазы было подтверждено экспериментально: прикрепив к вращающемуся участку помеченный флуоресцирующим красителем белок актин, похожий на длинную нить, ученые своими глазами увидели, что он вращается. И это несмотря на то, что соотношение размеров у них такое, как если бы человек размахивал двухкилометровой плетью.
Кинезин — это линейный молекулярный мотор, передвигающийся по клетке вдоль путепроводов — полимерных нитей. Будто портовый грузчик, он перетаскивает на себе всевозможные грузы (митохондрии, лизосомы), используя в качестве топлива молекулы АТФ.
Внешне кинезин похож на сплетенного из тонких веревок игрушечного «человечка»: он состоит из двух одинаковых полипептидных цепей, верхние концы которых сплетены и соединены вместе, а нижние расставлены в стороны и имеют на концах «ботинки» — глобулярные головки размером 7,5 х 4,5 нм. При движении эти головки на нижних концах поочередно отрываются от полимерной «тропинки», кинезин поворачивается на 180 градусов вокруг своей оси и переставляет одну из нижних «стоп» вперед. При этом если один его конец при движении тратит энергию (молекулу АТФ), то другой в это время высвобождает компонент для образования энергии, АДФ. В итоге получается непрерывный цикл подачи и траты энергии для полезной работы.
Как показали исследования, кинезин способен довольно бодро вышагивать по клетке своими «веревочными» ножками: делая шаг длиной всего 8 нм, за секунду он перемещается на гигантское по клеточным меркам расстояние в 800 нм, то есть делает 100 шагов в секунду. Попробуйте представить себе такие скорости в человеческом мире!
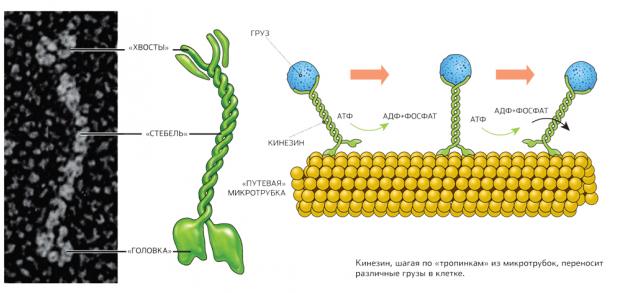
Кинезин, шагая по «тропинкам» из микротрубок, переносит различные грузы в клетке
Человеком, который подтолкнул научный мир к созданию нанороботов на основе биологических молекулярных устройств, стал выдающийся ученый-физик, нобелевский лауреат Ричард Фейнман. Его лекцию 1959 года с символичным названием «Там внизу еще много места» биоинженеры всего мира считают отправной точкой в этом нелегком деле.
Прорыв, позволивший перейти от теории к практике, случился в начале 1990-х годов. Тогда английские ученые из Университета Шеффилда, Фрэйзер Стоддарт и Нил Спенсер, и их итальянский коллега Пьер Анелли сделали первый молекулярный челнок — синтетическое устройство, в котором происходит пространственное перемещение молекул. Для его создания используют ротаксан — искусственное вещество, в котором кольцевая молекула (кольцо) нанизана на линейную молекулу (ось). Отсюда и название вещества: лат. rota — кoлесо и axis — ось. Ось в ротаксане имеет форму гантели, чтобы с помощью объемных групп на концах не позволять кольцу соскальзывать со стержня.
Челнок на основе ротаксана перемещает кольцевую молекулу вдоль линейной, на которой она держится, с помощью протонов (ослабляя или увеличивая водородные связи, удерживающие по центру кольцевую молекулу) и броуновского движения, толкающего вперед кольцо. Это похоже на брошенный в ручей резиновый мячик, привязанный к веревке: ослабили веревку (водородные связи) и стремительный ручей (броуновское движение) подхватит мяч и увлечет его вперед. Натянули веревку — мяч возвратится назад.

«Наномашина», «четырехколесная» молекула, созданная в 2005 году группой под руководством профессора Джеймса Тура (Университет Райса). Собственного мотора у нее нет, однако при нагревании поверхности до порядка 200 °C фуллереновые колеса начинают вращаться и машинка катится.
В 2010 году группа американских биоинженеров, Милан Стоянович и его коллеги, создали молекулярного наноробота, способного перемещаться по ДНК. В ходе эксперимента ученые смогли проследить, как их наноробот смог самостоятельно сделать 50 шагов и передвинуться на 100 нм. Робот, внешне напоминающий паука, может автономно выполнять несколько команд: «идти», «повернуть», «остановиться». По мнению авторов, он очень востребован в медицине в качестве доставщика лекарств в клетку.
В 2013 году английские и шотландские биоинженеры под руководством Дэвида Лея смогли создать первый в мире молекулярный наноконвейер: наномашину, способную собирать пептиды, короткие белки. В природе эту задачу выполняют рибосомы — органеллы, находящиеся в наших клетках. Биоинженеры взяли за основу для своей машины молекулу ротаксана и на ее «стержне» смогли собрать из отдельных аминокислот белок заданного свойства. Правда, в соревновании с природной сборкой белков в рибосоме искусственная молекулярная машина пока проигрывает: ей понадобилось 12 часов на присоединение каждого аминокислотного остатка, в то время как рибосомы справляются с этой задачей быстрее чем за секунду.
Несмотря на это, исследователи с оптимизмом рассматривают свою разработку. «Вы получаете машину, которая точно движется, поднимает молекулярные строительные блоки и ставит их вместе. Если природа делает это, почему не можем мы?» — отметил профессор Лей.
До сьогодні повідомлялось, що Феодосійська нафтобаза була зруйнована на 80%. На території окупованого Криму вночі проти неділі, 7 червня, було чутно вибухи і стрілянину, що виникли після оголошення повітряної тривоги. Попередньо отримані дані свідчать ...
У Тюмені сталася масштабна пожежа на Антипинському нафтопереробному заводі, яка, за даними пропагандистських ЗМІ, виникла через порушення технологічного процесу на одній із виробничих установок. Про це у суботу, 6 червня, пишуть російські ЗМІ, передают...